
2024年,诺贝尔化学奖颁给了蛋白质结构预测与设计领域。
这一奖项不仅是对蛋白质结构预测与设计技术的肯定,更催化了整个蛋白质赛道和生命科学领域的范式变革。
如今,AI+蛋白质研究不仅从单体结构预测走向了复合物预测,同时也从结构预测走向了功能创造。
海内外资本、企业纷纷向AI+蛋白质领域抛来了橄榄枝,创下多笔巨额融资。
2024年,诺贝尔化学奖得主David Baker创办的Xaira Therapeutics获得了超10亿美元种子轮融资,聚焦AI药物研发。
今年4月,另一位诺贝尔化学奖得主Demis Hassabis创办的Isomorphic Labs获得完成6亿美元融资,利用AlphaFold技术打造下一代药物引擎。
后AlphaFold时代,AI在蛋白质领域的影响已渗透至基础科研、医药研发、工业应用及技术工具开发等多个维度,并逐步打开了一个巨量的想象空间。
AI蛋白质赛道,全球有哪些主要公司?海外与国内公司又有什么不同?
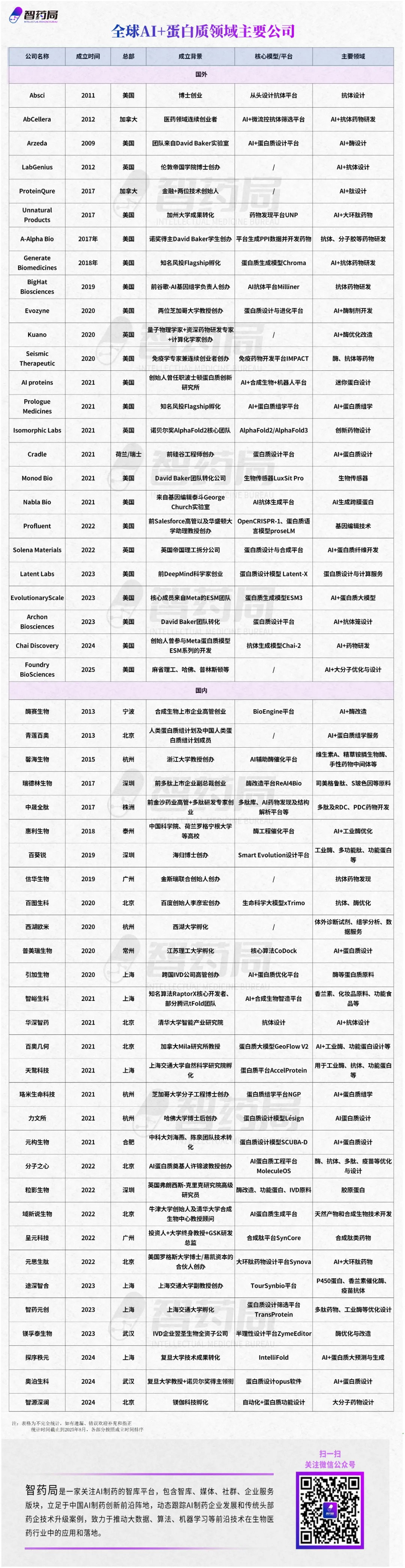
为此,智药局整理了全球AI+蛋白质赛道的玩家,希望能够更加清晰地呈现行业的整体情况。
据不完全统计,目前中国AI蛋白质企业共有30家,海外则拥有25家主要公司,主要集中在中国和美国。
从时间上看,2020年无疑是个分水岭,由Alphafold领衔的AI蛋白质预测浪潮成功“破圈”,在奠定了技术基础的同时,也进行了一波成功的市场教育,行业迎来一波持续三年的创业潮。
而2024年AI蛋白质技术获得诺贝尔奖后,标志着AI正式成为基础科研的核心方法论。结构生物学、化学与计算机科学的界限被打破,AI for Science这一理念兴起。
后续技术如AlphaFold3,则进一步拓展至更复杂的生物分子系统,为理解细胞机制提供原子级视角。
根据技术,这些公司主要分为两类:AI蛋白质预测与设计和AI蛋白质组学。
在蛋白质组学领域,AI的应用已经非常广泛且成熟。AI已经成为蛋白质组学数据分析的重要工具,许多商业化的蛋白质组学分析软件和服务都已经嵌入AI模块。
不过,当前制约蛋白质组学发展的核心仍然是提升通量和灵敏度,仍需开发类似NGS的革命性检测技术。
因此,AI在蛋白质组学领域更多是用来分析数据,并不触达核心,真正的关键在于硬件平台,即产生数据的手段。
蛋白质结构与设计领域,AI算法则是主要驱动力。
AlphaFold2 的成功本质是算法架构的革命,若仅依赖算力堆叠而无算法创新,无法实现原子级精度的预测。
如今,扩散模型、蛋白质语言模型等强大的生成式AI技术,可以学习蛋白质序列和结构的潜在规律,生成自然界不存在的、但具有稳定折叠和特定功能的蛋白质序列。
在下游应用领域,AI蛋白质技术的潜力几乎是无限的,其核心在于AI能够突破自然界蛋白质的限制,创造出拥有前所未有功能的蛋白质。
如今,AI正在渗透到多个关键领域,解锁整个药物研发、生物制造领域的潜力。
生物医药
当前,新药研发中抗体、肽类药物设计,以及疫苗开发都将受益于AI蛋白质技术。
尤其是抗体药物,2024年全球畅销药TOP10中,有7款都是抗体以及多肽类等大分子药物,而以AI蛋白质则作为底层技术有望革新这些药物发现。
通过精准预测药物靶点结构以及相互作用,AI可以帮助科学家设计出更具特异性、更高效的小分子或大分子抗体。
酶制剂和工业应用
酶是维持人类生命活动和工业生产不可或缺的生物催化剂。在工业生产中,酶作为高效的生物催化剂,被广泛应用于多个领域,包括医疗、农业、食品、能源、材料等。
近年来,蛋白质设计正在工业酶领域发力,AI蛋白质设计技术能够设计出超高性能的工业用酶。
不过,酶的稳定性和活性之间的关系非常复杂,从头开始设计功能酶是蛋白质工程中的一个重大挑战。不过近年来多家公司在数据稀缺的情况下,依旧完成了酶工程领域的突破。
例如海外专门从事酶设计与改造的公司Arzeda,能够对酶的特征、蛋白质能量以及代谢途径的高通量预测,已经与联合利华、武田、英国石油等顶级公司合作。
国内包括酶赛生物、馨海生物、分子之心等也均在深度布局AI酶优化与设计技术,并且和国内外头部企业达成合作,共同赋能医药以及生物制造等领域。
高校与大厂成为创新主力
从成立背景上看,由于AI蛋白质研究涉及到生命科学最核心的领域,因此海内外公司的技术溯源后基本都来自高校实验室。
在海外,美国和英国正在引领全球计算蛋白质的发展,例如诺奖得主David Baker从上世纪90年代就开始从事计算蛋白质研发,团队积累了深厚的蛋白质工程与算法经验,目前已经转化出十几家AI蛋白质相关公司。
除开高校外,来自大厂的衍生公司也是海外AI蛋白质创新生态的重要一环。
例如DeepMind拆分的顶级独角兽Isomorphic Labs,Meta蛋白质团队衍生出来的EvolutionaryScale、Chai Discovery等。
国内AI蛋白质公司主要来自于高校以及研究院成果转化,包括来自中科大、复旦大学、上海交通大学等高校,由大厂引领的创新生态较为缺乏。
本土转化的公司外,近年来华人科学家回到中国创业也逐渐增多。
例如“AI蛋白质折叠奠基人”许锦波教授归国创办分子之心,加拿大Mila研究所唐建教授回国打造百奥几何等,为国内AI蛋白质赛道注入了新动能。
海外偏向于技术突破,中国更注重产业落地
技术路线上,海外在AI基础研究方面有更深的积累,更偏向基础大模型,如DeepMind发布的AlphaFold3 、Arc Institute开发的生物学大模型Evo2等,都在引领全球科研以及行业发展。
同时美国拥有成熟的风险投资生态,科技巨头、医药巨头以及顶尖风投都愿意押注高风险技术,并且提供大规模资金支持。这让初创公司可以长期保持高投入,进行大量技术性的探索,重新定义技术边界。
例如前Meta蛋白质团队推出开源蛋白质语言模型ESM3,OpenAI支持的Chai Discovery推出蛋白质模型Chai-1、抗体设计模型Chai-2等。
国内公司也在致力于AI生物学技术创新,例如百图生科推出生命科学基础大模型xTrimo V3,覆盖蛋白质、DNA、RNA等领域。
除此之外,国内创新及支持体系有待完善,中国研究团队则更注重将AI应用于具体产业化场景。AI技术正在嵌入现有产业链,例如优化工业酶、诊断试剂、合成生物等可快速商业化的领域。
例如AI蛋白质公司天鹜科技成功交付了二十余款蛋白质设计项目,拓展至多个领域,包括创新药、体外诊断、营养保健、食品饮料、美容护肤等。
蛋白质几乎承担了人类所有的生命活动,其重要性贯穿生命科学的每一个层面。
诺奖得主David Baker曾经写道,蛋白质设计正在从类似于从石器时代过渡到铁器时代的技术进步,这个节点正是AlphaFold2的出现。
后AlphaFold2时代,基于深度学习的蛋白质设计方法层出不穷。
人们希望通过计算机得到更可控、更有规律、更有表现力的蛋白质设计方法,该领域也开始受到学界和工业界的重视,相关研发团队和公司也开始涌现。
尤其大模型的出现深刻改变了蛋白质领域乃至生命科学的游戏规则,使得在数据驱动的生命科学研究与理性设计成为可能。
不过,和AI赋能小分子研究的快速进展相比,蛋白质研究的AI应用确实面临更多深层挑战,进展相对缓慢。
目前全球进入临床的AI赋能的药物仍然以小分子为主。原因在于小分子不仅数据更加完善,且高通量筛选技术成熟。
而蛋白质功能依赖多维度动态信息,现有数据库与实际生物活性存在偏差,导致从头设计具有特定功能的蛋白质仍然有很长的路要走,整个流程仍然存在很多不确定性。
如今,AI蛋白质赛道正处于技术突破到商业化落地的关键期,随着AI设计方案在安全性和有效性超越传统方法,相信赛道将迎来商业化爆发。
文章来自于微信公众号“智药局”,作者是“王苏”。